口腔科器械����、眼科器械、醫(yī)美器械是非常熱門醫(yī)療器械細(xì)分類別���,伴隨著電子產(chǎn)品在生活中的深度����、廣度參與��,以及人口老齡化進(jìn)程���,眼科器械近年及未來很長一段時(shí)間都是增量需求����。本文為大家說說用于干眼癥治療的液脈動(dòng)干眼治療儀臨床試驗(yàn)設(shè)計(jì)實(shí)例��,一起看正文�����。
口腔科器械、眼科器械�����、醫(yī)美器械是非常熱門醫(yī)療器械細(xì)分類別�,伴隨著電子產(chǎn)品在生活中的深度、廣度參與�,以及人口老齡化進(jìn)程,眼科器械近年及未來很長一段時(shí)間都是增量需求�。本文為大家說說用于干眼癥治療的液脈動(dòng)干眼治療儀臨床試驗(yàn)設(shè)計(jì)實(shí)例,一起看正文���。
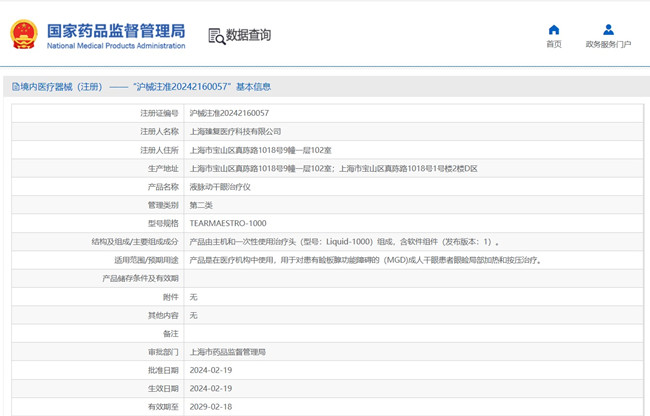
液脈動(dòng)干眼治療儀臨床試驗(yàn)設(shè)計(jì)實(shí)例
醫(yī)療器械注冊(cè)人提交140例患者臨床研究方案以及總結(jié)報(bào)告�����,以驗(yàn)證該產(chǎn)品的安
全性及有效性����。參考中國干眼專家共識(shí):治療(2020年)�,中國干眼專家共識(shí):檢查和診斷(2020年)確定用于療效評(píng)價(jià)的主要指標(biāo)和客觀指標(biāo)。
觀察時(shí)間點(diǎn):治療后30±5天��。
主要有效性評(píng)價(jià)指標(biāo)為:非接觸式淚膜破裂時(shí)間(NIBUT)�����;
次要有效性評(píng)價(jià)指標(biāo)為:眼表疾病綜合 OSDI���、Schirmer I 試驗(yàn)數(shù)值�、
角膜熒光素染色(CFS)轉(zhuǎn)陰率和 CFS 評(píng)分����、最佳矯正視力(BCVA)、
瞼板腺萎縮評(píng)分(MGDS)
安全性評(píng)價(jià)指標(biāo)為:不良事件發(fā)生�����、嚴(yán)重不良事件發(fā)生率�����。
液脈動(dòng)干眼治療儀臨床試驗(yàn)結(jié)果顯示:
(1)主要有效性評(píng)價(jià)指標(biāo)
兩組治療后30±5天的非接觸式淚膜破裂時(shí)間(NIBUT)存在顯著差異����,
試驗(yàn)組NIBUT高于對(duì)照組。
(2)次要有效性評(píng)價(jià)指標(biāo)
兩組治療后30±5天的試驗(yàn)組和對(duì)照組眼表疾病綜合OSDI評(píng)分��、
Schirmer I試驗(yàn)數(shù)值�、角膜熒光素染色(CFS)轉(zhuǎn)陰率和CFS評(píng)分存在
顯著差異���,Schirmer I試驗(yàn)數(shù)值、角膜熒光素染色(CFS)轉(zhuǎn)陰率高于
對(duì)照組��;眼表疾病綜合OSDI評(píng)分����、CFS評(píng)分則低于對(duì)照組(兩組評(píng)分越
低越好)。
(3)安全性評(píng)價(jià)指標(biāo)
本研究試驗(yàn)期間共發(fā)生不良事件 6 例���,無受試者因不良事件退出����。試驗(yàn)組共發(fā)生3例次不良事件�,包括中度結(jié)膜充血1例,眼瞼疼痛2例��;對(duì)照組共發(fā)生3例次不良事件��,包括中度結(jié)膜充血2例��,眼瞼疼痛1例�,兩組的不良事件發(fā)生率差異沒有顯著的統(tǒng)計(jì)學(xué)意義(P=1.0) ,并且隨訪中受試者均自行緩解��。提示試驗(yàn)組(液脈動(dòng)治療)與對(duì)照組(眼部熏蒸加以人工瞼板腺按摩)的安全性差異無統(tǒng)計(jì)學(xué)意義。
如有液脈動(dòng)干眼治療儀臨床試驗(yàn)設(shè)計(jì)服務(wù)或是其他醫(yī)療器械臨床試驗(yàn)設(shè)計(jì)服務(wù)需求�,歡迎您隨時(shí)方便與杭州證標(biāo)客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡(luò)����,聯(lián)系人:葉工,電話:18058734169�����,微信同��。